
CaCO3 có kết tủa không ?
CaCO3 là một hợp chất hóa học vô cơ có tên gọi là Canxi Cacbonat được hình thành khi Canxi liên kết với gốc Cacbonat. Chất này thường được tìm thấy dưới dạng đá ở khắp nơi trên thế giới, là thành phần chính trong mai/vỏ của các loài sò, ốc hoặc vỏ của ốc.
CaCO3 tồn tại tự do trong tự nhiên dưới dạng tinh thể và rất ít tan trong nước nên CaCO3 có kết tủa khi cho Ion Ca2+ tiếp túc với gốc Cacbonat. Một số ví dụ điển hình sau đây:
Ca(OH)2 + CO2 → CaCO3. [Ca(OH)2 dùng dư hoặc CO2 dùng vừa đủ tạo kết tủa]
Ca(OH)2 + H2CO3 → CaCO3 + H2O
CaCO3 có kết tủa màu gì ?
CaCO3 có kết tủa màu trắng khi tồn tại trong dung dịch kết tủa CaCO3 thường xuất hiện thành từng mảng nhỏ lơ lửng trong dung dịch.
CaCO3 có liên quan tới nhiều bài tập hóa học vô cơ ở dạng khó và thường thấy nhất là bài toán sục CO2 vào dung dịch Ca(OH)2 tạo thành kết tủa sau đó tiếp tục sục khí CO2 thì thấy kết tủa tan dần. Những bài toán này đã có cách giải ở bài viết riêng, các em có thể tìm kiếm trên website hoahoc24h.com nhé! Chúc các em học tốt.!
Phân Tích Quá Trình Phản Ứng Trong Lò Cao và Vai Trò của Nhiệt Độ
CaCO₃ là muối cacbonat có cấu trúc tinh thể ion, gồm cation Ca²⁺ và anion CO₃²⁻. Trong môi trường nhiệt độ cao của lò cao, đặc biệt ở vùng trên 800-1000°C, CaCO₃ mất tính ổn định do ion CO₃²⁻ kém bền nhiệt, dễ bị phân hủy giải phóng khí CO₂. Chính phản ứng này là bước khởi đầu để tạo ra CaO - chất chủ lực trong tạo xỉ.
Quá trình phân hủy CaCO₃ theo vùng nhiệt độ
Vùng 200-600°C: CaCO₃ còn bền vững
Trong khoảng nhiệt độ thấp ở phần trên của lò cao, CaCO₃ tồn tại ở trạng thái gần như bền vững. Liên kết trong ion CO₃²⁻ tuy kém bền hơn so với oxit kim loại, nhưng vẫn chưa đạt tới mức năng lượng để phân rã. Tại vùng này, CaCO₃ chỉ bị sấy khô và chuẩn bị cho quá trình biến đổi ở nhiệt độ cao hơn.
Vùng 600-900°C: khởi đầu sự phân hủy
Khi đi sâu hơn xuống thân lò, năng lượng nhiệt tăng dần. Các dao động nội phân tử trong ion CO₃²⁻ trở nên mạnh, làm cho liên kết C-O trong nhóm cacbonat bắt đầu suy yếu. Tuy nhiên, sự phân hủy vẫn diễn ra chậm và chưa hoàn toàn. Vai trò của vùng nhiệt này chủ yếu là giai đoạn chuẩn bị, làm cho CaCO₃ trở nên hoạt hóa.
Vùng trên 900-1000°C: phân hủy hoàn toàn
Đây là ngưỡng nhiệt độ quyết định. Ion CO₃²⁻ không còn ổn định, dẫn đến phản ứng phân hủy:
CaCO₃ (r) → CaO (r) + CO₂ (k)
- CaO hình thành là chất rắn có cấu trúc ion mạnh, bền nhiệt, hoạt tính hóa học cao.
- CO₂ sinh ra hòa trộn cùng khí lò (CO, N₂, H₂…), và khi gặp than cốc ở vùng nhiệt độ cao hơn, một phần CO₂ tiếp tục phản ứng với C để tạo CO, bổ sung khí khử cho quá trình khử quặng sắt.
Vùng trên 1200-1600°C: tạo xỉ
CaO sinh ra lập tức phát huy vai trò quan trọng nhất: phản ứng với tạp chất oxit axit, điển hình là SiO₂ có trong quặng sắt hoặc tro than cốc. Phản ứng điển hình:
CaO (r) + SiO₂ (r) → CaSiO₃ (l)
Sản phẩm là xỉ lỏng CaSiO₃, có nhiệt độ nóng chảy thấp. Lớp xỉ này nổi lên trên bề mặt gang lỏng, đóng vai trò:
- Bảo vệ gang nóng chảy khỏi bị oxi hóa trở lại.
- Thu giữ và loại bỏ tạp chất.
- Tạo điều kiện duy trì môi trường khử trong lò.
Vai trò của nhiệt độ trong toàn bộ quá trình
- Cung cấp năng lượng phá vỡ liên kết trong CO₃²⁻: Liên kết C-O trong anion cacbonat khá bền, chỉ khi đạt ngưỡng trên 900°C thì phân hủy mới diễn ra triệt để.
- Điều khiển sự cân bằng phản ứng: Phản ứng phân hủy CaCO₃ là phản ứng thu nhiệt. Theo nguyên lý Le Chatelier, khi tăng nhiệt độ, cân bằng sẽ dịch chuyển mạnh về phía tạo sản phẩm (CaO và CO₂).
- Liên kết với chu trình khí khử trong lò: CO₂ sinh ra từ phân hủy CaCO₃ không chỉ là sản phẩm phụ mà còn tham gia phản ứng với C ở vùng nhiệt cao để duy trì nguồn cung CO.
- Đảm bảo tính lỏng của xỉ: Ở nhiệt độ trên 1200-1600°C, sự hình thành xỉ CaSiO₃ và các hợp chất silicat khác duy trì trạng thái lỏng, dễ tách ra khỏi gang, nhờ đó quá trình luyện gang đạt hiệu quả tối ưu.
Ngoài ra, thiết kế lò cao với chiều cao lớn và phân vùng nhiệt độ từ trên xuống dưới nhằm tạo ra sự tuần hoàn nhiệt: nguyên liệu đi xuống, khí nóng đi lên, tối ưu hóa việc trao đổi nhiệt và làm cho mỗi tầng nhiệt độ chỉ diễn ra những phản ứng phù hợp. Điều này giúp tiết kiệm năng lượng và đạt hiệu suất cao nhất.
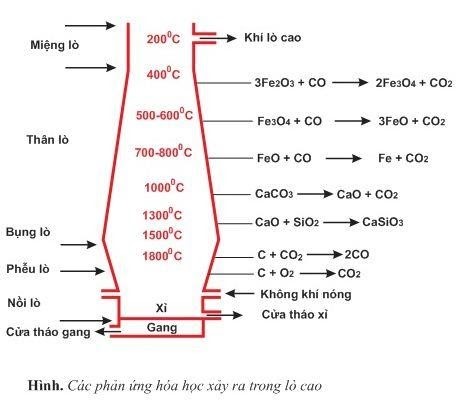
Bên cạnh phản ứng khử oxit sắt, các phản ứng khác như:
- Phản ứng giữa C và CO₂ ([C + C{O_2} to 2CO]) ở ~1800°C, duy trì lượng khí CO cần thiết cho các phản ứng khử.
Tất cả các phản ứng này đều được sắp xếp tuần tự về nhiệt độ, phù hợp với cơ chế hoạt động tối ưu của từng giai đoạn vật liệu.


